第19届国际输血协会(ISBT)血小板免疫学研讨会概况
第19届国际输血协会(ISBT)血小板免疫学研讨会于2018年6月在加拿大多伦多召开,会议就以下6项目(Exercise)展开讨论:
(1)4例临床案例和1例献血者样本的血清学评估,及胎母/新生儿同种免疫血小板减少症(FNAIT)诊断的实验室实践调查。
(2)一例临床案例特异性评估(抗-HLA)
(3)5例DNA盲样样品的基因分型检测
(4)使用PAKLx商品试剂盒的实验分析
(5)用于MAIPA方法的检测抗-HPA-3抗体的血小板抗原谱细胞制品
(6)MAIPA的重点挑战:多种用于检测抗-HPA-15的抗-CD109单克隆抗体
全球共29家实验室参加本届研讨会,其中28家实验室提交了各自的实验结果。中国有来自南宁输血医学研究所、浙江血液中心和广州血液中心的3家实验室参加了本次研讨会。
第19届国际输血协会(ISBT)血小板免疫学研讨会6个项目的研讨结果如下:
(1)4例临床案例和1例献血者样本的血清学评估,及胎母/新生儿同种免疫血小板减少症(FNAIT)诊断的实验室实践调查。
Part 1 血小板抗体特异性检测(盲样检测)
本项目提供5份盲样血清样本(含4例临床案例和1例献血者血清样本),要求参与实验室采用各自实验室的常规检测方法鉴定血清中所含的血小板抗体特异性。
结果:
Sample | Antibody specificity (Consensus/majority results) |
1 | Anti-HPA-1b and anti-HLA |
2 | Anti-HPA-2b and anti-HLA |
3 | Anti-HPA-5b and anti-HLA |
4 | Anti-GPIV |
5 | Anti-HPA-3a |
结果显示参加项目的实验室对抗-HPA-2b和抗-HPA-5b特异性抗体的检测结果完全一致(100%),特别是在样本2和样本3。此外各实验室对抗-HPA-1b和抗-GPIV抗体特异性检测结果极佳,一致性结果分别为96.43%和89.29%。较多的问题在样本5的检测,仅有4个实验室(14.29%)能够正确检测鉴定到抗-HPA-3a抗体,78.57%的参加实验室在该样本的检测结果为阴性。尽管对于一些实验室由于样本量限制原因无法进行进一步检测分析,但这无疑表明并非所有抗体都易于鉴定,因此大部分实验室需要进一步优化抗-HPA-3a的检测鉴定方法。
Part 2 FNAIT的实验室管理调查
通过调查问卷的形式了解各实验室对FNAIT的实验室管理情况
结果:
调查结果表明,用于鉴定抗-HPA抗体的方法和HPA型别的评估是一致的。各实验室所报告的临界值(cut-off值)明显不同的。此外,对抗体定量检测的实验室,对抗体量的评估和使用的方法不同。这些对抗体含量评估的实验室结果报告是不一致的。
其他领域的多种实践可能从测试指南中获益,包括所推荐的对妊娠期间对抗体的检测时间和频率到妊娠指数的方法。在对自身抗体的重要性、报告及重新测试方面达成了较好的共识,并在实验室的质量改进上具有极大的相关性,这将成为将来工作组的一个主要方向。
(2)一例临床案例特异性评估(抗-HLA同种抗体导致的FNAIT)
对一例抗-HLA介导的FNAIT进行抗体特异性检测和评估
结果:
表1 抗体特异性检测结果
抗体类别 | 检测结果 |
抗-HPA | 阴性 |
抗-HLA | 阳性 特异性:抗-HLA-A3,-B7 |
表2案例HLA基因分型检测结果
HLA基因型 | |
母亲 | HLA-A*11, A*24, B*18, B*51 |
父亲 | HLA-A*03, A*03, B*07, B*35 |
新生儿 | HLA-A*03, A*11, B*07, B*18 |
该案例是罕见的由抗-HLA抗体介导的FNAIT。因此具有非常重要的临床意义。这对夫妇的第一次怀孕生产,新生儿因严重颅内出血而死亡。第二次怀孕也受到影响,但是新生儿可以分娩没有受伤。其第一和第二胎新生儿均出现严重血小板减少,血小板计数分别为5和7。
在FNAIT案例中,并非总是会对抗-HLA进行检测。 但是,此案例已证明抗-HLA在FNAIT的严重直接影响。
(3)5例DNA盲样样品的基因分型检测
本项目提供5份DNA样本,要求参加实验室对该DNA样本进行HPA- 1~15基因分型。
结果如下:
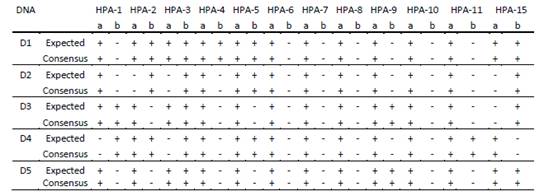
结果显示,所有参加实验室均对最重要的HPA系统(HPA-1,-2,-3,-5和-15)进行基因分型检测,另约42-68%的实验室对较低发生率抗体的血小板抗原系统(HPA-4,-6和-11)进行检测。在参加实验室中,HPA基因分型检测展现了极佳的重复性(99.3%)。目前,实时定量PCR是HPA基因分型的最用常方法。很少实验室开展HPA-12至-14和HPA-16-28的基因分型检测。他们评论部分报告了5个DNA样本在这些HPA系统的基因型结果均为aa,一实验室报告在样本D1、D3和D4具有HPA-6a变异体。
(4)使用PAKLx商品试剂盒的分析血小板同种抗体的特异性
该项目主要测试PAKLx的检测能力
结果:
总体而言,在检测含有强抗体滴度的样本时,PAKLx和MAIPA之间存在良好的相关性。而随着样本的稀释,PAKLx的敏感性降低。表明抗体特异性的检测仍具有挑战,尤其是在较低抗体滴度时,如HPA-3(exercise 1)和HPA-5。
(5)用于MAIPA方法检测抗-HPA-3抗体的血小板制品
主要检测所提供的用于MAIPA检测的血小板制品(血小板抗原谱细胞)的有效时间。
所提供血小板抗原谱细胞制品的HPA型别:
血小板谱细胞 | HPA型别 |
P1 | HPA-1a/1a, 3a/3a |
P2 | HPA-1a/1a, 3b/3b |
结果:
用于本实验项目的样品具有过高的抗体反应性,为达到本实验目的要求,我们需要对样品进行稀释后使用,使这些样品更充分地呈现实验结果。根据获得的结果,在测试时间段(24h,48h和72h),使用所提供的血小板抗原谱细胞制品,检测结果无差别或者至少差别无统计学意义。我们仍无法清楚的证明随着时间的延长该血小板抗原谱细胞制品对抗体反应性的影响。同样,虽然观察到随着时间的延长血小板抗原谱细胞具有反应性降低的趋势,但该实验项目仍无法回答蛋白质在制备后仍可在血小板表面保存多长时间的问题。
(6)MAIPA的重点挑战:多种用于检测抗-HPA-15的抗-CD109单克隆抗体
比较和评估4种不同来的抗-CD109克隆抗体(clones 1-4)产品的有效性,优化使用MAIPA检测抗-HPA-15抗体的敏感性。
结果:
在使用相同的样品(S11和S12均为抗-HPA-15b阳性血清)和血小板谱细胞的情况下,与各实验室内部的CD109单克隆抗体比较,使用Clones 1-4对S11和S12检测结果较弱或为阴性。
使用Clones 1-4的结果通常是不一致的,并且与样品S11和S12中预期的抗-HPA-15b抗体特异性结果无关联。提供的两个样本中S11表现较差,各参加实验室普遍没有检测到其抗体特异性。
相反地,使用各实验室内部的CD109单克隆抗体对S11和S12进行检测时,有11/23(48%)的实验室获得较高的OD值,并能够检测样本中含有抗-HPA-15b抗体。
结论:
首先使用Clones 1-4获得的不良结果很可能是由于克隆本身的因素,但目前具体原因仍不清楚。其次使用相同单克隆TEA2/16各实验室获得的结果中,明显可见使用CD109的MAIPA方法仍缺乏标准性。最后,对于参加本项目的实验室,很明显的仍面临单克隆抗体的挑战,部分实验室使用所提供的克隆仍能够检测到HPA-15b抗体,虽然OD值相对较低,但总体来说他们的MAIPA方法仍更可靠。这对于将来的合作研究中,确定使用CD109单克隆抗体进行MAIPA检测提供最佳实践是有益的。
作者:李丽兰
扫一扫 手机端浏览
